Lab. Clin. Pract., 19(1) : 11-13 (2001)
最近の話題
生 化 学
マイクロ化学分析システム
― マイクロマシン技術 ―
早稲田大学理工学部 電子・情報通信学科
庄 子 習 一
1. は じ め に
わが国の最も得意とする分野である半導体微細加工技術を用い集積回路以外の電子素子や機械素子の製作を行うマイクロマシン技術のさまざまな分野への応用が進展している.化学計測や生化学計測において,この技術は最初にイオン選択性電界効果トランジスタ(ISFET)やマイクロバイオセンサなど,電気化学的な検出方式を用いる化学,生化学マイクロセンサの製作に応用された.次に,シリコンやガラス基板上へのガスクロマトグラフィーや液体クロマトグラフィー用の微小なカラムの製作や,マイクロアクチュエータを用いて超小型のバルブやポンプなどのマイクロ流体制御素子の製作に同様な技術が用いられ,最近ではマイクロ化された化学分析システム(Micro/Miniaturized Total Analysis Systems: μTAS)に関する研究が盛んに行われるようになった1), 2).化学分析システムの各要素をマイクロマシン技術により小型化し,基板上に集積化することは,システムの小型化,低価格化,無効体積の減少を可能にする.また,計測に必要なサンプルや試薬の量や分析で生じる廃液の量も大幅に低減できる.さらに,測定時間の短縮やシステム全体の消費電力低減などの利点もある.以下,マイクロ化学分析システムの事例についてその概要を述べる.2. マイクロ機械素子を用いたμTAS
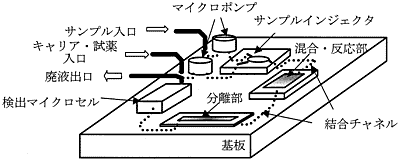
最初に研究が盛んに行われたのはマイクロマシン技術で製作されるマイクロポンプやマイクロバルブなどの機械式マイクロ流体制御素子を用い従来の化学分析システムを小型化したものである3).フローインジェクション分析(FIA)を例としたμTASの概念図を図1に示す.これは1枚の基板上に集積化されたシステムの概念図で試料導入機構やキャリア溶液,サンプルの流れを制御するポンプおよび試薬との混合/反応器,成分分離部,センサ部からなっている.それぞれの要素をマイクロ化し,内部に流路が形成された基板に並べ,Oリングなどを介して接続するハイブリッド型システムが提案されている1).現状では分析システムの一部をマイクロ化された要素で置き換えたシステムが実用化されるており,そのマイクロ化の有効性が証明されている.しかし,総合的なシステムとしての実用例はまだ少なく,マイクロバルブやマイクロポンプなどのマイクロ流体制御素子が実用上重要な研究課題となっている.図1 マイクロ機械素子を用いたハイブリットμTASの概念図2)
3. チップキャピラリー電気泳動型μTAS
ヒューマンゲノムプロジェクトにおいて,並列化されたキャピラリー電気泳動システムの導入により,人間のDNA配列解析が飛躍的に進展した.最近,この方法に用いられるガラスキャピラリーの代わりに,マイクロマシン技術を用いてガラスやプラスチック基板上に微細な流路(キャピラリー)を形成したチップキャピラリー電気泳動(チップCE)システムが盛んに研究されている4).図2はガラス基板上に形成された電気泳動分析システムの概念図で,電気泳動を行う流路とキャリア,試薬などの液体導入用流路がガラス基板上に形成されており,流路の入口と出口の液溜めに電極が形成されている.キャリア液へのサンプルの導入には電圧を印加するだけで流れを制御できる電気浸透流を用いるため,機械的なポンプやバルブが必要なく構造が非常に簡単である.DNA分析に関しては蛍光分析を用いる場合が多く,光源・レンズ・フィルタなどからなる光学式の検出装置が用いられている.このようなシステムでは流路の断面積を小さくすることにより分離効率を高め,流路の長さを短くすることにより分析時間を短縮することが可能である.蛍光や吸光など光学的な分析では,光源からの光を微小な流路に焦点を合わせ,発生する光を集めて分光器に送るレンズ系が必要で,どうしても検出系が大きくなる.このため,検出装置を共通としてキャピラリーを並列にして分析の効率化を図る研究が進んでいる(図3).今は流路の構造や配置を工夫することにより,一つの光学系で48〜96本のCEを短時間に計測するシステムが開発されている5).分子量の大きいサンプルの分析には分解能が高い質量分析法が適しており,アミノ酸,ペプチド,タンパク質,酵素などの分析に用いられている.チップCE型のシステムで分離したサンプルを直接既存の質量分析器に導入して検出する研究も進められている6).|
図2 平面基板上に作られたキャピラリー電気 泳動分析システムの概念図2) 
|
図3 バッチ型μTASおよびサンプル前処理 システムの概念図2) 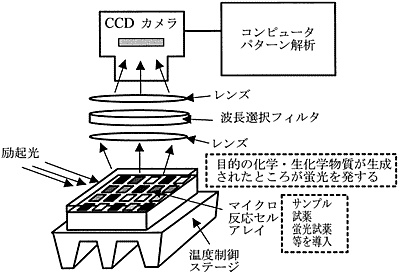
|
4. バッチ型μTAS
DNA分析が進展した背景にはDNAの増幅方法であるPolymerase Chain Reaction (PCR)法の確立がある.この方法は2本鎖DNAの単鎖への分離,DNA合成酵素による2本鎖のDNAの合成を繰り返し,DNA増幅を行うものである.この反応過程はそれぞれ違う三つの温度で起こり,熱サイクルを高速に切り替えればDNA増幅が短時間で行える.このため,マイクロマシーニングを用いて熱容量の小さいマイクロ反応セルを作るとDNA増幅が早く行える.マトリックス状に形成されたマイクロ反応セルを用い,DNA生成の検出に蛍光酵素を用いてPCRにより増幅された特定のDNAを光学的に検出する装置が製作されている7).多数のマイクロ反応セルが形成されたシリコンチップからの蛍光信号をCCDカメラで一括して観察することにより,効率の良いDNA分析が実現される.このようなマイクロシステムは並列化されたチップCEシステムのサンプルの前処理システムとしても有効である.5. DNAチップを用いたμTAS
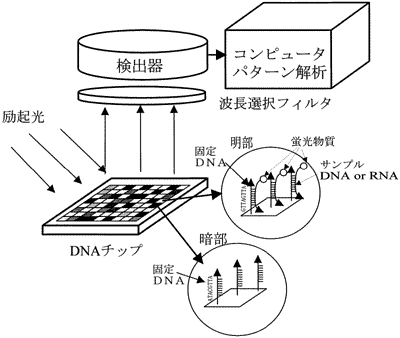
DNAチップとは図4に概念図を示すように組み合わせの異なる比較的短い塩基列の単鎖のDNAプローブを基板上にマトリックス状に形成したものである.DNA鎖の形成には点着装置が開発されているが,フォトリソグラフィー技術を応用しているものもある8).このチップに蛍光酵素をラベルしたサンプルを導入すると,DNA配列の一致したものだけがDNAプローブと強く結合し基板上に固定される.その後,未結合のサンプルを洗浄したあと励起光を照射すると固定されたサンプルがある部分だけが蛍光を発する.この蛍光パターンをコンピュータ解析することにより,極めて短時間にDNAの配列を決定することが可能であり,DNAの多形や異形の分析に有効であると考えられている.図4 DNAチップを用いた分析システムの概念図2)
6. お わ り に
μTASについてシステム構成の違う四つのタイプ紹介したが,それぞれ利点をもち応用分野が異なっている.マイクロ機械素子を用いたμTASは構造が複雑であるため,いまだにその要素や素子レベルの研究が行われている状況である.チップCE型μTASは北米を中心に盛んに研究されており,DNA分析から,酵素,プロテオーム,抗原・抗体をターゲットとした生化学分析へと応用の範囲が広がっている.いずれも前処理や分析試料の導入機構など周辺の装置が必要で,総合的な分析システムとしてのマイクロ化を実現するためにはマイクロ流体制御デバイスの開発が不可欠である.今後,電気,機械分野のシーズと化学,生化学分野のニーズが適合するよう研究開発者とユーザの交流をますます密にすることが望まれる.文 献
1) 庄子習一:マイクロ化学分析システム,電子情報通信学会論文誌,J81-C-I, 385-393 (1998).2) 庄子習一:μTASその現状と将来,精密工学会誌,65 (5): 655-658 (1999).
3) Shoji, S.: Fluids for Sensor Systems, Topics in Current Chemistry (Eds. A. Manz and H. Becker), Vol. 194, pp. 164-188, Springer Verlag, Heidelberg, 1998.
4) Effenhauser, C. S.: Integrated Chip-Based Microcolumn Separation Systems, Topics in Current Chemistry (Eds. A. Manz and H. Becker), Vol. 194, pp. 51-82, Springer Verlag, Heidelberg, 1998.
5) Mathies, R. A., et al.: DNA Analysis with Capillary Array Electrophoresis Microplates, Proc. Micro Total Analysis Systems, μTAS98, pp. 1-6, 1998.
6) Wang, X.-Q., et al.: Polymer-Based Electrospray Chips for Mass Spectrometry, Tech. Dig., IEEE Micro Electro Mechanical Systems, MEMS-99, pp. 523-528, 1999.
7) Woudenberg, T. M., et al.: High Density PCR and Beyond, Proc. Micro Total Analysis Systems, μTAS96, pp. 55-59, 1996.
8) Anderson, R. C., et al.: Polynucleotide Arrays for Genetic Sequence Analysis, Topics in Current Chemistry (Eds. A. Manz and H. Becker), Vol. 194, pp. 117-129, Springer Verlag, Heidelberg, 1998